基于微生物生長曲線測定儀研發(fā)導(dǎo)管尖端的自動化培養(yǎng)鑒定方法
留置血管內(nèi)導(dǎo)管是為患者實施診療時常用的醫(yī)療操作技術(shù)。隨著各種導(dǎo)管在臨床廣泛的應(yīng)用,導(dǎo)管相關(guān)的感染也越來越多。血管導(dǎo)管相關(guān)感染(Vessel CatheterAssociated Infection,簡稱VCAI)是指留置血管導(dǎo)管期間及拔除血管導(dǎo)管后48小時內(nèi)發(fā)生的原發(fā)性、且與其他部位感染無關(guān)的感染,包括血管導(dǎo)管相關(guān)局部感染和血流感染。目前臨床常用的導(dǎo)管的類型包括中心靜脈導(dǎo)管、PICC、臍血管導(dǎo)管、完全植入式靜脈輸液港、血液透析導(dǎo)管、外周動脈導(dǎo)管、漂浮式肺動脈導(dǎo)管等。這些導(dǎo)管的植入是一種侵襲性操作,操作過程中污染,護理不當(dāng),放置的時間過長、菌血癥等原因都會引起導(dǎo)管相關(guān)感染。
據(jù)報道,聚氯乙烯、硅膠制品等導(dǎo)管可以粘附大量微生物,從而增加感染幾率。隨著導(dǎo)管留置時間延長,導(dǎo)管在其內(nèi)的留置會使血液中的纖維蛋白及血清蛋白沉淀聚集在導(dǎo)管表面,反而起到了保護病原體的作用。綜上,病原體可沿導(dǎo)管表面向體內(nèi)蔓延生長,繁殖到一定數(shù)量時釋放人血就會出現(xiàn)菌血癥、敗血癥的相關(guān)臨床癥狀,有感染導(dǎo)致休克死亡的風(fēng)險。因此,及時確定是否血管導(dǎo)管相關(guān)感染并快速選擇合理有效的抗感染藥物是治療成功的關(guān)鍵。
為明確導(dǎo)管相關(guān)感染,需要進行導(dǎo)管尖端培養(yǎng)以明確診斷,鑒別致病菌。目前常見的檢測方法包括以下步驟:1)用無菌剪刀剪下導(dǎo)管尖端,2)將剪下的導(dǎo)管尖端放在無菌容器中送至專業(yè)微生物檢驗實驗室,3)在實驗室內(nèi)將待測導(dǎo)管尖端在血平皿上作滾動涂布接種,4)將血平皿在恒溫培養(yǎng)箱中培養(yǎng)約20h,5)取出血平皿通過觀察有無菌斑來判斷該導(dǎo)管尖端外部是否被可培養(yǎng)細(xì)菌污染。如果需要檢測導(dǎo)管尖端內(nèi)部是否被污染,則需要采用超聲震蕩無菌生理鹽水沖洗導(dǎo)管尖端,然后將沖洗水涂在血平皿上接種,再進行其它的操作步驟。目前檢測導(dǎo)管及導(dǎo)管尖端是否被病原體污染的主要問題有四個,一是即使有細(xì)菌粘附污染,在接種時也不一定能(全部)從待測導(dǎo)管尖端上脫離并接種到血平皿上,因而易造成假陰性誤判;二是操作繁瑣,結(jié)果嚴(yán)重依賴微生物檢驗專業(yè)操作人員的個人技能;三是周期長,效率低,培養(yǎng)結(jié)果在72小時后才能反饋給臨床;這導(dǎo)致針對致病菌的針對性治療延后了至少72小時。四是致病原鑒定無法在床旁等現(xiàn)場實施。
目前醫(yī)療行業(yè)急需簡便高效、快速準(zhǔn)確檢測導(dǎo)管相關(guān)感染及床旁快速藥敏試驗的新技術(shù)。
導(dǎo)管尖端的自動化培養(yǎng)鑒定步驟:
步驟1:一次性檢測管中預(yù)裝入蛋白胨水,將待測導(dǎo)管尖加入到所述一次性檢測管中,將一次性檢測管封口;
步驟2:然后將一次性檢測管插入微生物生長曲線自動化測定儀器中的檢測通道;
步驟3:通過微生物生長曲線自動化測定儀器測定的細(xì)菌生長曲線形狀判斷目標(biāo)導(dǎo)管尖是否有細(xì)菌或真菌定植
采用八通道電容耦合非接觸式電導(dǎo)率檢測器作為傳感單元,采用一對同軸銅氣缸作為致動器電極和拾取電極,構(gòu)成電容耦合的非接觸式電導(dǎo)率檢測器的工作通道。在將充滿含有導(dǎo)管尖的培養(yǎng)液試管插入工作通道后,將交流電壓施加到致動器電極上,以電容耦合到水介質(zhì)中。致動器電極和拾取電極與絕緣管和介質(zhì)形成兩個耦合電容(Cw)。損耗電容(Cs)產(chǎn)生于兩個電極通過空氣(Cs)之間的直接電容耦合。該水介質(zhì)相當(dāng)于一個電阻器接收站。介質(zhì)的表觀電導(dǎo)率(直流電壓信號)在拾取電極上獲得;其大小與水介質(zhì)中離子載流子的濃度和遷移率成正比。如果導(dǎo)管尖存在細(xì)菌或者真菌,細(xì)菌或真菌細(xì)胞將在所需的溫度下增殖和生長。細(xì)菌的生長轉(zhuǎn)化了不帶電或弱帶電的底物,酵母、肽和糖轉(zhuǎn)化成高電荷的最終產(chǎn)物,如氨基酸、醛、酮、酸等代謝物,提高水介質(zhì)的電導(dǎo)率。通過電容耦合的非接觸式電導(dǎo)率檢測器,每間隔30秒自動在線收集水介質(zhì)的表觀電導(dǎo)率。由于電導(dǎo)率的變化而不是絕對值與細(xì)菌生長的動力學(xué)過程成正比,我們使用算法計算每個試管中水介質(zhì)的電導(dǎo)率變化值(即歸一化表觀電導(dǎo)率值NACV)如下:
NACVn=ACVn-ACV0
式中,NACVn為n點收集的實時NACV;ACVn為n點收集的表觀電導(dǎo)率值;ACV0為孵育開始時收集的初始表觀電導(dǎo)率值。然后通過繪制NACVs為孵育時間的函數(shù)來生成s型CCS生長曲線。當(dāng)導(dǎo)管尖沒有任何細(xì)菌真菌時,生長曲線為一條直線(沒有s型CCS生長曲線)。
細(xì)菌或者真菌在生長代謝的過程將分解導(dǎo)電性較差的有機大分子物質(zhì),生成導(dǎo)電性較好的小分子物質(zhì)和離子,造成混合體系導(dǎo)電能力的增加,即混合體系電導(dǎo)C值的增加。這種電導(dǎo)的增加過程可以通過電子微生物生長分析儀實時在線監(jiān)測并生成C-t曲線。從電子微生物生長分析儀自動報告的細(xì)菌生長C-t曲線形狀直接讀出定性檢測結(jié)果:正峰,且電導(dǎo)率值(NACV)>0.02V,說明目標(biāo)細(xì)菌或菌群生長;水平線,說明細(xì)菌沒有生長。
快速藥敏試驗為頭孢他啶管和頭孢他啶-克拉維酸管在培養(yǎng)45000s內(nèi),兩管電導(dǎo)率值差值(NACV’)>0.02V。
導(dǎo)管尖端的自動化培養(yǎng)鑒定方法工作過程為:
將從臨床送檢的導(dǎo)管尖端放置到預(yù)先裝滿蛋白胨水的專用檢測管中,將檢測管封口后插入電子微生物生長分析儀,電子微生物生長分析儀全自動在線監(jiān)測并繪制出非接觸電導(dǎo)(C)-時間(t)曲線。從電子微生物生長分析儀自動報告的細(xì)菌生長曲線形狀直接讀出結(jié)果(培養(yǎng)45000s內(nèi)):電導(dǎo)率值(NACV)>0.02V,說明導(dǎo)管尖存在細(xì)菌或真菌;電導(dǎo)率值(NACV)<0.02V或水平線,說明沒有細(xì)菌或真菌生長。細(xì)菌的生長代謝過程由電子微生物生長分析儀全自動在線監(jiān)測并繪制出非接觸電導(dǎo)(C)-時間(t)曲線。測定結(jié)束后根據(jù)C-t曲線的形狀及電導(dǎo)率值判斷導(dǎo)管尖是否有細(xì)菌生長。
測定金黃色葡萄球菌(ATCC25923)標(biāo)準(zhǔn)菌株在導(dǎo)管尖內(nèi)定植能否被檢測。
步驟一、啟動電子微生物生長分析儀(ER832型,澳大利亞eDAQ公司產(chǎn)品)和專用計算機。在檢測軟件窗口設(shè)置溫度、采集頻率、采集次數(shù)、激勵頻率和激勵強度參數(shù)分別為38℃、1分鐘/次、1200次、30KHz和80%,預(yù)熱10分鐘,待用。
步驟二、采用單通道移液器(大龍公司產(chǎn)品,量程為0-200μL)將含107
CFU/mL金黃色葡萄球菌(ATCC25923)的200μL LB液體培養(yǎng)基打入導(dǎo)管尖中,將導(dǎo)管尖放入已經(jīng)預(yù)裝有2mL蛋白胨水(廣州迪景微生物科技有限公司)的一次性檢測管(青島谷峰實驗儀器有限公司產(chǎn)品,U型,材質(zhì)為聚丙烯,外徑5mm,內(nèi)徑4.5mm,管長170mm),然后采用無菌膠塞封住管口。同樣,將200μL無菌LB液體培養(yǎng)基打入導(dǎo)管尖中,將導(dǎo)管尖放入已經(jīng)預(yù)裝有2mL蛋白胨水的一次性檢測管并封口,作為陰性對照;
步驟三、將上述兩個檢測管分別插入電子微生物生長分析儀的檢測通道,并開始測定細(xì)菌C-t曲線。
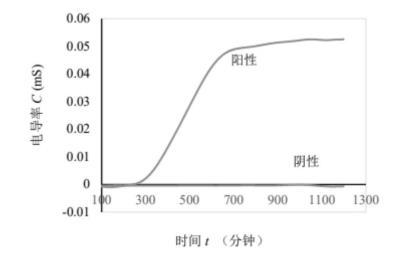
步驟四、對應(yīng)于待測金黃色葡萄球菌(ATCC25923)和陰性對照的C-t曲線如圖1所示。其中陰性對應(yīng)一條直線,說明檢測體系未被污染。金黃色葡萄球菌(ATCC25923)對應(yīng)一條正峰(即細(xì)菌生長代謝且結(jié)果造成血液電導(dǎo)增加),說明體系中細(xì)菌能夠正常生長代謝。
測定肺炎克雷伯菌(ATCC700603)標(biāo)準(zhǔn)菌株快速藥敏試驗。
步驟一、同實施例1步驟一。
步驟二、采用單通道移液器將含肺炎克雷伯菌(ATCC700603)待測菌株107
CFU/mL200uL打入兩個導(dǎo)管尖中,將含有待測菌株的導(dǎo)管尖所在的蛋白胨水作為待測液分別加入已經(jīng)預(yù)裝含有頭孢他啶(16mg/L)、頭孢他啶-克拉維酸(16/4mg/L)的蛋白胨水中的一次性檢測管,然后采用無菌膠塞封住管口。同樣,將200μL超純水轉(zhuǎn)入一個同樣已經(jīng)預(yù)裝有蛋白胨水的檢測管并封口,作為陰性對照;頭孢他啶-克拉維酸管與頭孢他啶管比較,可初步判斷是否產(chǎn)超廣譜內(nèi)酰胺酶。
步驟三、將上述三個檢測管分別插入電子微生物生長分析儀的一個檢測通道,并開始測定細(xì)菌C-t曲線。
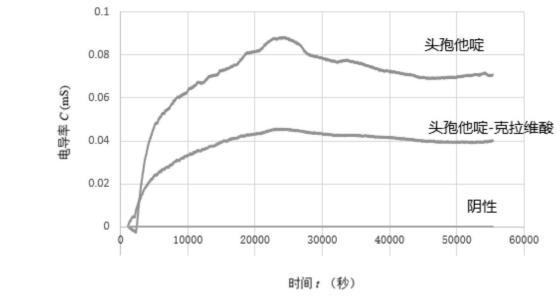
步驟四、對應(yīng)陰性對照、含有頭孢他啶(16mg/L)、頭孢他啶-克拉維酸(16/4mg/L)的蛋白胨水的C-t曲線如圖2所示。其中陰性對應(yīng)一條直線,說明檢測體系未被污染。含有頭孢他啶(16mg/L)比頭孢他啶-克拉維酸(16/4mg/L)在培養(yǎng)45000s內(nèi),兩管電導(dǎo)率值差值(NACV’)>0.02V。說明體系中細(xì)菌能夠正常生長代謝且產(chǎn)生超廣譜β內(nèi)酰胺酶(即具有耐藥性)。通過是否產(chǎn)生超廣譜β內(nèi)酰胺酶判斷細(xì)菌是否具有耐藥性。
超廣譜β內(nèi)酰胺酶(ESBL)是一類能水解青霉素類,頭孢菌素類以及單環(huán)類抗生素的β-內(nèi)胺酶,其活性能被某些B-內(nèi)酷胺酶抑制劑抑制。能產(chǎn)生ESBL的細(xì)菌即為ESBL(+)菌,可對上述多種抗生素產(chǎn)生耐藥;
肺炎克雷伯菌為一種革蘭氏陰性桿菌,其最重要的耐藥機制是產(chǎn)生超廣譜β-內(nèi)酰胺酶;
頭孢他啶-克拉維酸(頭孢他啶與克拉維酸聯(lián)用)的原因:革蘭氏陰性桿菌產(chǎn)生的超廣譜β內(nèi)酰胺酶的活性可以被β內(nèi)酰胺酶抑制劑,比如克拉維酸所抑制。
相關(guān)新聞推薦
1、不同溫度和pH對白三葉草鏈格孢菌菌落生長的影響【實驗結(jié)果】
2、冷鮮豬肉中熱殺索絲菌生長動力學(xué)模型和貨架期預(yù)測模型構(gòu)建——摘要、材料與方法
3、不同儲藏溫度下鮮豬肉細(xì)菌菌落總數(shù)測定及Logistic生長曲線函數(shù)模型構(gòu)建(三)
