微生物代謝物抑制 HIF-2α-神經酰胺途徑,減輕飲食誘導的肝脂肪變性
代謝功能障礙相關的脂肪變性肝病(MASLD)影響著四分之一的人口,對所有社會都構成了重大的健康和經濟負擔。MASLD包含多種肝臟表現,從肝脂肪變性到更具侵襲性的代謝功能障礙相關脂肪性肝炎(MASH),后者以壞死炎癥和纖維化為特征,可進展為肝硬化和肝細胞癌(HCC)。減緩MASLD的進展,尤其是逆轉已建立的MASH,是臨床治療的重點。鑒于其復雜的病理學和目前缺乏批準的醫療干預措施,積極的飲食和生活方式方法仍然是其管理的主要選擇,但由于依從性差而受到限制。調整飲食攝入量及進餐頻率和飲食時間窗口,已成為改善和延緩疾病發作和衰老的有力工具。限時喂養(TRF)需要在不限制熱量攝入的情況下將每日食物攝入限制在4至12小時的窗口內,被認為是一種有效的飲食和生活方式干預措施,可以改善和推遲疾病的發作。研究表明,TRF可以減輕體重,提高胰島素抵抗,抑制肝脂質積累。然而,導致TRF益處的特定分子機制仍然難以捉摸。腸道菌群的組成是調節宿主代謝的關鍵因素。腸道微生物群的組成和功能容易受到飲食特征的影響,例如脂質的數量和組成。食物過度消費、食物短缺,甚至飲食周期的變化都可能影響腸道菌群。TRF可以部分恢復小鼠高脂飲食(HFD)攝食引起的腸道菌群周期性波動,增加腸道菌群多樣性,影響宿主代謝,表明腸道微生物群可能在TRF的益處中發揮重要作用。微生物代謝物被認為是微生物群與宿主之間通信的關鍵介質,維持宿主的生理功能。
腸道微生物群和微生物代謝物是否有助于TRF對MASLD/MASH的影響仍有待探索。這項研究使用10小時TRF方案作為對MASLD患者和小鼠模型的干預措施,以探索TRF可以改善這種情況的潛在機制。發現10小時TRF后腸道菌群中的瘤胃球菌(R.torques)增加,該物種的定植足以模擬TRF對MASLD/MASH的有益影響。從機制上講,文章發現R.torques通過其微生物代謝產物2-羥基-4-甲基戊酸(HMP)抑制腸道HIF-2α-神經酰胺軸來改善MASLD/MASH。總的來說,這些結果確定了R.torques及其相關代謝物之一HMP在TRF對MASLD/MASH的有益作用中的作用,表明R.torques或HMP可能作為益生菌或作為MASLD/MASH的藥物治療開發。
研究亮點
1.TRF相關細菌R.torques通過其代謝物HMP改善MASLD/MASH
2.rtMor是一種在R.torques中鑒定出的酶,可產生HMP
3.HMP可以作為TRF模擬物,解決對禁食方案的依從性差的問題
圖文賞析
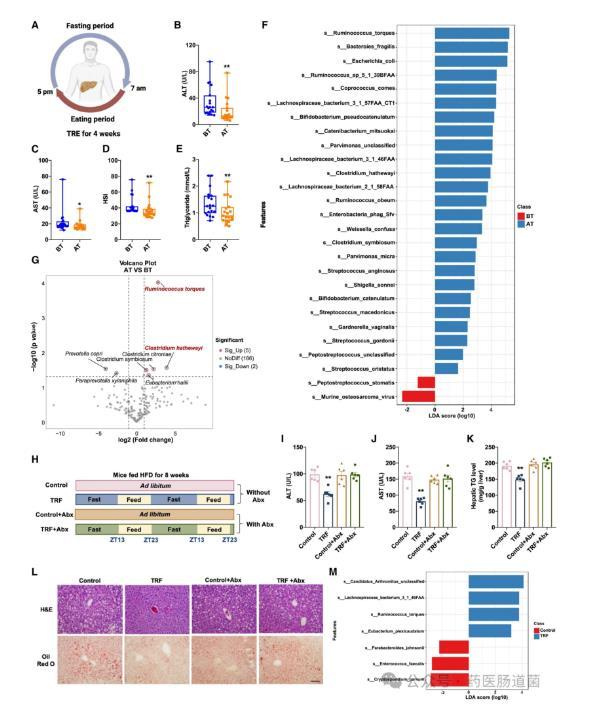
圖1腸道菌群的變化與TRF對MASLD的益處有關
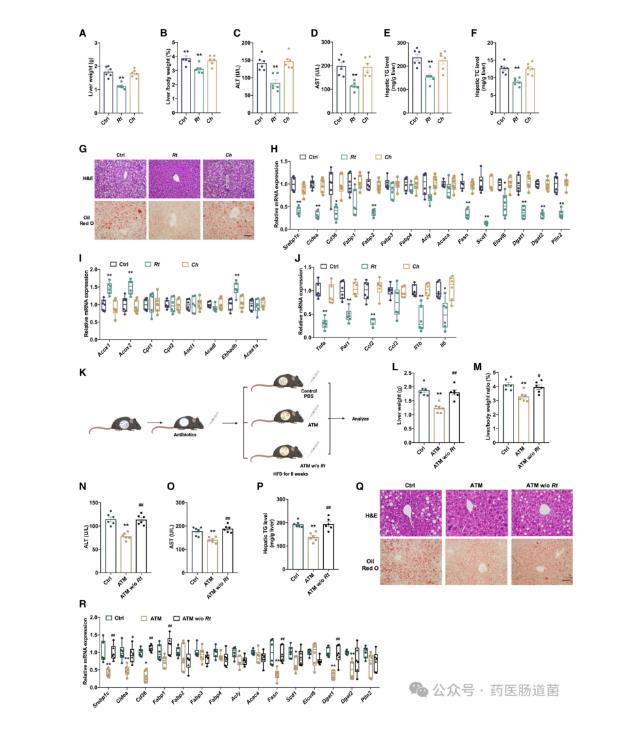
圖2 R.torques是促成TRF對MASLD益處的關鍵細菌種類
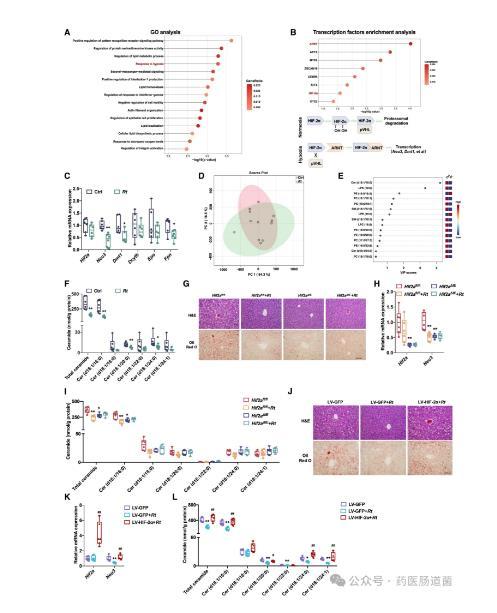
圖3 HIF-2α-神經酰胺信號轉導介導R.torques對MASLD的有益影響
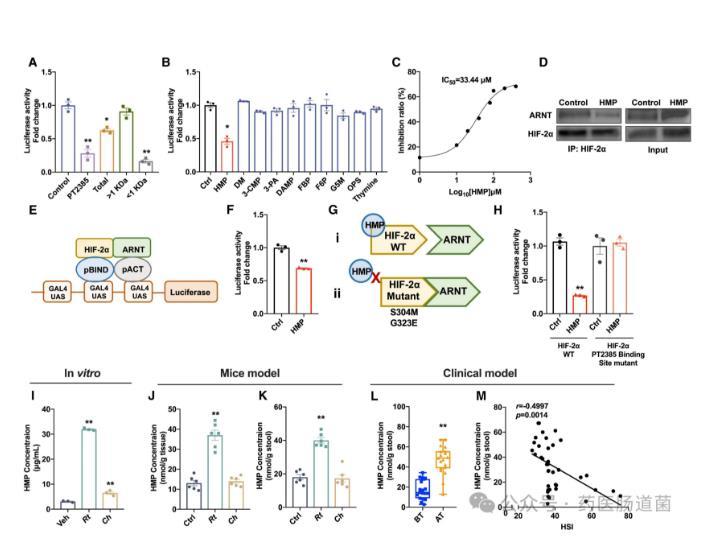
圖4 HMP是HIF-2α的內源性抑制劑
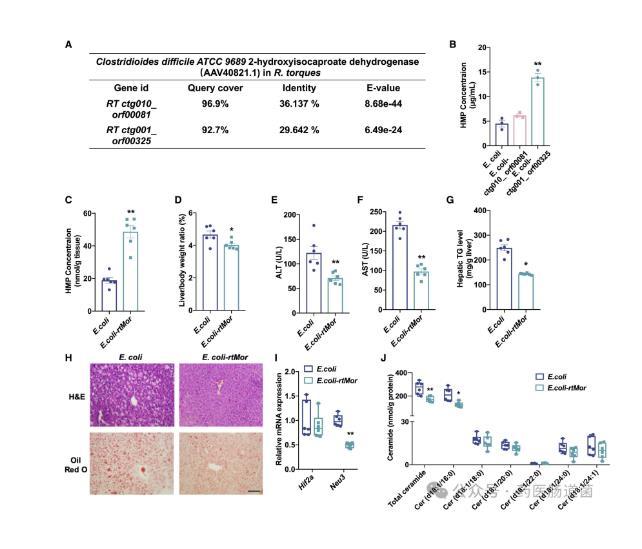
圖5 HMP通過HIF-2α-神經酰胺軸改善HFD誘導的MASLD

圖6 R.torques或HMP的給藥可改善小鼠的MASH
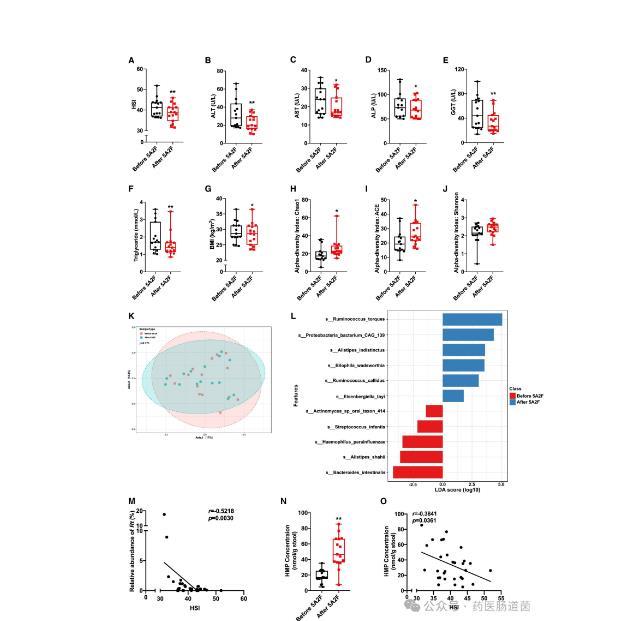
圖7 5A2F干預可增加R.torques和HMP水平
總結與意義
研究發現R.torques衍生的代謝物HMP作為一種TRF模擬物,可以抑制腸道HIF-2α-神經酰胺信號傳導,從而減輕飲食誘導的肝脂肪變性。HMP來源于L-亮氨酸,很久以前就被發現是由厭氧菌產生的。然而,在瘤胃球菌中尚未發現催化以4-甲基-2-氧代戊酸為中間體形成HMP的還原酶。雖然許多細菌可以產生HMP,富含TRF的R.torques是改變最顯著的HMP產生細菌,其升高的HMP水平可以通過抑制腸道HIF-2α-神經酰胺軸來改善MASLD。目前沒有報道HMP與生理代謝有關,而研究表明,HMP作為一種潛在的治療劑MASLD/MASH具有改善作用。事實上,通過對細菌進行生物工程來生產HMP可能會提供一種“藥物細菌”的方法來改善這種難以治療的疾病。確定TRF方案促進了R.torques的增長,通過HMP-HIF-2α-神經酰胺軸有助于改善MASLD/MASH的改善。這些發現加深了對腸道共生菌調節宿主代謝疾病發展機制的理解,同時提供了新的策略來模仿對大多數人來說可能難以堅持的禁食飲食制度。
相關新聞推薦
1、MDCK單克隆細胞復蘇活率、生長狀態、生長速度和生長形態研究
3、模擬失重條件下大腸埃希菌轉錄組測序、差異基因及富集分析結果(二)
