快速藥敏檢測方法、發展現狀|拉曼光譜在RAST領域中的應用(二)
3拉曼光譜技術在RAST領域中的應用
3.1基于單細菌分子表型的RAST
基于單細菌分子表型的RAST可以省去細菌增殖所需時間。目前,基于單細胞水平的快速分子表型的藥敏檢測,主要依賴于活細菌對重水(D2O)的代謝攝入,生成細菌內部的生物分子,比如脂質和蛋白質等,通過檢測C-D峰的強度可以實現抗菌藥物MIC的快速檢測。
C-D峰位于拉曼光譜的2 040~2 300 cm-1波段,該波段通常在未進行D2O標記的細菌中無可檢測到的拉曼峰,具有高特異性。見圖1。此外,在含有D2O的培養基中生長的細菌C-D峰的強度變化與活細菌的代謝活性呈正相關。
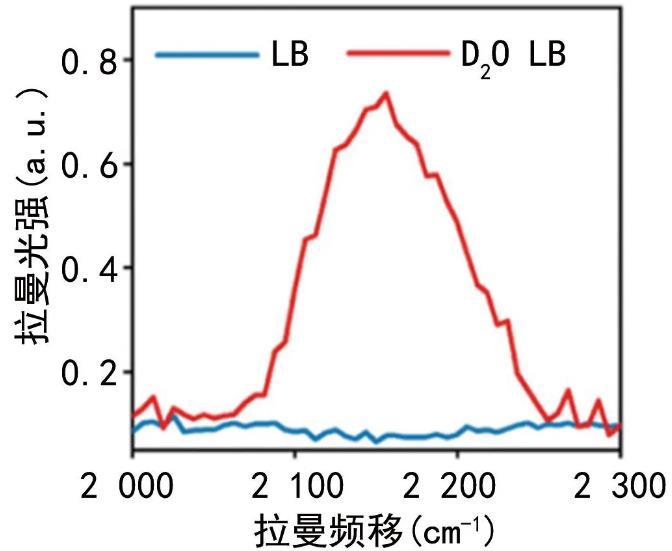
圖1銅綠假單胞菌在正常和含D2O的培養基中培養
任何活細菌的代謝都需要水,因此,在含有D2O的培養基中生長的活細菌都會生成代謝表征的C-D峰,這決定了C-D峰可作為分辨單細菌細胞代謝活動的通用生物標志物。在基于培養的藥敏檢測方法中,細菌增殖一代的時間比開始出現代謝表征的時間長,而且不同種細菌的生長時間差異也會使藥敏時間難以縮短,因此,基于C-D峰的單細胞拉曼藥敏檢測方法在RAST領域中有著極好的應用前景。
在目前的研究中,運用單細胞拉曼技術進行MIC的快速測定大致分為3步:(1)細菌在含有不同濃度梯度抗菌藥物的培養基中先孵育1~2 h;(2)按體積比向培養基中加入D2O(目前報道30%~100%D2O濃度),同時保證培養基濃度和藥物濃度與初始一致,繼續孵育30 min左右;(3)根據耐藥組和敏感組的相對C-D比,即C-D/(C-H+C-D)來設定cut off值以測定MIC。
3.1.1運用CRS技術進行RAST
TAO等證明了基于D2O活菌代謝標記的單細胞拉曼光譜可以檢測細菌對抗菌藥物的反應,2 040~2 300 cm-1波段的C-D拉曼帶可作為單細菌代謝活性的通用生物標志物。YANG等開發了適用于臨床尿液標本直接藥敏檢測的單細胞拉曼光譜技術,基于活菌的D2O代謝摻入,通過相對C-D比設置S/R截止值用于藥敏結果判讀,達到了從接收尿液標本到結果讀取總檢測時間縮短至2.5 h,且準確度高的效果。YUAN等將31株伊麗莎白菌分別與8種不同濃度抗菌藥物和40%D2O共孵育,4 h即可測定抗菌藥物的MIC,除頭孢吡肟外,其他7種抗菌藥物的單細胞拉曼藥敏結果與金標準藥敏結果一致率為94%。在該研究中,頭孢吡肟所測藥敏結果與金標準結果不一致可能是因為不生長但代謝活躍的細菌存在,這種特性可能會影響藥敏結果的準確性,也會成為細菌感染治療后復發的根源。因此,臨床可以通過單細胞拉曼藥敏檢測技術來評估抗菌藥物療效,更好地指導臨床給藥。
3.1.2運用SRS技術進行RAST
快速準確的藥敏試驗對于多藥耐藥菌的安全、有效和環境友好型治療至關重要。ZHANG等利用飛秒受激拉曼散射成像對經過70%D2O培養基和不同濃度抗菌藥物孵育后的細菌進行單細胞成像,在不到2.5 h測定了14種抗菌藥物對臨床常見8種病原菌的MIC值,與金標準藥敏結果的符合率為94.6%。此外,該研究制備了模擬尿液和血液標本,通過直接過濾的方法分離細菌進行藥敏檢測,準確度良好。此外,ZHANG等在單細胞水平上,通過SRS成像監測抗菌藥物作用下的D2O活菌代謝摻入,在2.5 h內測得抗菌藥物的單細胞代謝失活濃度。該方法還適用于尿液或血液等復雜生物標本的直接RAST。
3.2基于多細菌分子表型的RAST
雖然基于單細菌分子表型的RAST方法具有一定優勢,但由于細菌是活體,同種菌的不同個體狀態在不同時間或空間可能不同,這會影響藥敏結果的準確性。因此,有研究者開發了基于多細胞水平分子表型檢測的RAST方法,這種方法主要依賴于SERS技術。CHANG等開發了集成膜過濾和SERS活性襯底的微流控系統,微通道內腔室的膜可過濾和濃集細菌,注射泵將培養基、抗菌藥物和洗滌液等注入其中,在過濾室中培養細菌,細菌釋放的代謝物被輸送到附著SERS襯底的微通道中進行檢測,藥敏檢測時間明顯縮短。FU等篩得一種帶負電荷的適配子,與細菌特異性結合,利用粗糙金屬納米顆粒的信號放大作用,測定了大腸埃希菌O157∶H7和金黃色葡萄球菌在不同濃度抗菌藥物作用下的拉曼光譜,首次發現735 cm-1可作為標志峰位置,基于此峰強度的變化,在1 h內可測得藥物的MIC。HILTON等將納米銀顆粒印在SERS紙傳感器上,利用便攜式拉曼光譜儀對不同β-內酰胺類抗菌藥物耐藥的大腸埃希菌進行檢測,在2.5 h內即可完成大腸埃希菌的耐藥分析。新型RAST技術匯總見表1。
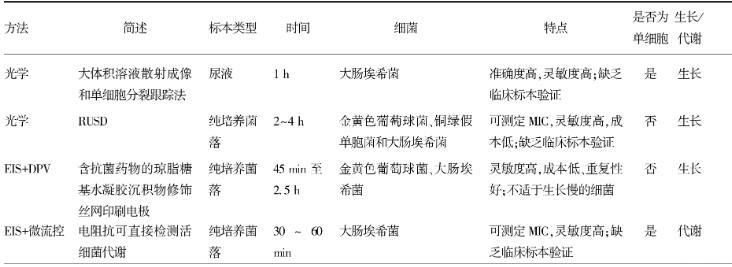
表1新型RAST技術匯總
4結論與展望
基于細菌生長和代謝表型的RAST技術相較于傳統藥敏方法的檢測時間明顯縮短,其中,運用拉曼光譜技術在細菌代謝表型水平進行RAST具有很好的應用前景。
雖然微流控、電阻抗和SYBR GreenⅠ活菌染色等技術平均藥敏檢測時間為1 h左右,但適用的細菌和抗菌藥物都比較局限,也無法識別菌群中的異耐藥菌,而且檢測結果的準確性缺乏大標本量的驗證。此外,這些基于生長的藥敏檢測對細菌的初始接種量有要求,而且細菌在剛接種到培養基中會經歷1~3 h的遲緩期,很難檢測到數量上的微弱變化,還易受到細菌本身狀態和環境等因素的影響。
基于RNA測序的藥敏檢測目前只對環丙沙星作用于大腸埃希菌有研究,雖然其屬于細菌代謝表型檢測的RAST,但操作復雜,初始菌量要求高,難以滿足臨床要求。基于單細菌和多細菌代謝表型的RAST技術準確度高、靈敏度高,但仍有許多不足之處:(1)缺乏大規模臨床分離株和抗菌藥物的驗證;(2)缺乏標準化的檢測流程、不能做質控和室間比對等;(3)細菌個體的異質性會影響單細菌藥敏檢測的準確性;(4)對于SERS的藥敏檢測,增強基底合成復雜,容易受到殘留培養基和其他成分的干擾,可重復性低等;(5)適用的標本類型局限于純培養菌落、尿液和全血標本,而對于復雜的痰液、糞便等標本的直接藥敏檢測鮮有研究。
未來還需要對基于細菌生長和代謝表型檢測的RAST技術進行大量的臨床分離株和抗菌藥物驗證,并對檢測結果的準確性進行評估;其次是標本處理流程的標準化,做好質控和室間比對,提高檢測的可重復性和臨床適用性;進行拉曼光譜藥敏檢測時要引入合適的內標,消除復雜因素對檢測的影響,也可以將拉曼光譜與電阻抗、微流控、化學染色等技術相結合,開發更快、更準確、重復性更好的RAST方法,實現在復雜標本中直接進行細菌快速鑒定及藥敏檢測。
相關新聞推薦
1、產單核細胞李氏桿菌噬菌體分離、超離、宿主譜鑒定及生長曲線繪制(三)
2、稻花香馫香型根霉曲、中高溫大曲和高溫大曲的酶活力和微生物數量統計(上)
3、焦化污染場地中萘降解菌株AO-4鑒定、生長、降解機理及環境條件帶來的影響(二)
