E-test法多黏菌素藥敏條用于臨床腸桿菌科體外藥敏檢測(一)
腸桿菌科細菌是革蘭陰性菌中非常重要的一類微生物,是引起臨床感染的重要病原菌之一,可致化膿性疾病、肺炎、腦膜炎、菌血癥以及傷口、泌尿道和腸道的感染。多黏菌素是從多黏類芽孢桿菌(Paenibacillus polymyxa)培養液中獲得的多肽類抗生素,根據化學結構共分為5型,其中僅B和E應用于臨床,主要用于治療革蘭陰性菌所致的全身多位點感染,因其較嚴重的腎毒性及神經系統毒性曾經一度被棄用。近年來,隨著抗生素的廣泛應用,腸桿菌科細菌對多種抗菌藥物產生了耐藥性,多黏菌素類作為治療的最后選擇又被應用于臨床。本研究結合最新2018版美國臨床實驗室標準化研究協會(CLSI)M100-S28標準,收集了2018年上半年河南省人民醫院、河南省中醫一附院、鄭州大學二附院臨床分離腸桿科菌株887株,同時采用E-test法和微量稀釋法進行體外藥敏試驗,考察兩種方法的一致性,為臨床腸桿菌科細菌體外多黏菌素藥敏試驗提供參考,指導臨床合理進行體外藥敏檢測。
1材料和方法
1.1菌株來源
本研究收集了2018年1月—6月河南省人民醫院、河南省中醫第一附屬醫院、鄭州大學第二附屬醫院臨床常規分離腸桿科菌株887份,其中埃希菌屬331株,克雷伯菌屬207株,沙門菌屬103株,志賀菌屬112株,其他屬腸桿菌134株(腸桿菌屬57株,檸檬酸桿菌屬48株,耶爾森菌屬13株,摩根菌屬7株,布丘菌屬6株,西地西菌屬3株)。質控菌株采用ATCC標準菌株:大腸埃希菌(ATCC25922)、產酸克雷伯菌(ATCC700324)、肺炎克雷伯菌(ATCC700603)、肺炎克雷伯菌肺炎亞種(ATCC13883)、腸炎沙門菌(ATCC13076)、鼠傷沙門菌(ATCC14028)、索氏志賀菌(ATCC25931)、霍氏腸桿菌(ATCC700323)、人蒼白桿菌(ATCC49687)、人蒼白桿菌(ATCCBAA-749)均源于鄭州安圖生物工程股份有限公司。
1.2試劑
多黏菌素B藥敏條由鄭州安圖生物工程股份有限公司提供,血瓊脂平板、90mm Mueller-Hinton(MH)平板均由鄭州安圖生物工程股份有限公司提供。多黏菌素B抗菌藥物為標準品,購自中國食品藥品檢定研究院;MH肉湯購自于BD醫療器械(上海)有限公司。
1.3方法
按照多黏菌素B藥敏條說明書進行操作。待測菌株和質控菌株分純過夜,挑取純菌落制備濁度為1.5×108CFU/mL濃度菌液,用無菌棉簽浸蘸菌液涂布于90mm MH平板表面,放置5min后,用真空吸筆吸取藥敏條放置于平板上然后放置(35±1)℃孵育,孵育16~20h后,讀取抑菌圈邊緣與藥敏條相交位置處的最低抑菌濃度(minimal inhibitory concentration,MIC)值。微量稀釋法的操作和判讀參照CLSI標準:在96孔酶標板的2~12孔各加100μL肉湯培養基;加100μL含64μg/mL抗生素的肉湯培養基至第1和第2孔中;從第2~12孔作對倍稀釋;加100μL含有105CFU待檢細菌新鮮肉湯培養基于每一孔;設立陽性對照孔,陰性對照孔,抗生素對照孔;密封酶標板,(35±1)℃環境下孵育20~24h,當陽性對照孔明顯渾濁時,記錄MIC值。EA(essential agreement):指待測方法與對比方法(或參考方法)MIC值在±1個稀釋倍數范圍內的一致性。藥敏條與微量稀釋法比對超過±1個稀釋倍數時進行復測,復測仍然超過±1個稀釋倍數判為不一致。
1.4統計學分析
采用SPSS 18.0統計軟件,計數資料采用χ2檢驗,P>0.05為無顯著性差異。
2結果
2.1質控菌株檢測結果
本次質控選用的9株ATCC標準菌株,均重復3次檢測,其中僅大腸埃希菌ATCC25922在CLSI有質控范圍為0.5~2μg/mL,采用微量稀釋法和藥敏測定MIC值均在±1個稀釋倍數范圍內,符合性能要求,具體數據見表1所示。
2.2樣本結果分析
共計887株腸桿菌的比對中,873株用藥敏條和微量稀釋法測定MIC值在±1個稀釋倍數的范圍內。其中完全一致的有594株(594/887,66.97%),±0.5個稀釋倍數的有170株(170/887,19.17%),±1個稀釋倍數的有86株(86/887,9.70%)。有45株菌的MIC值超出了±1個稀釋倍數,EA%為94.93%(842/887),針對第一次測定不符合的經復測確認,有36株菌測定結果仍然不符合,即糾正后的EA%為95.94%(851/887),結果見表2所示。
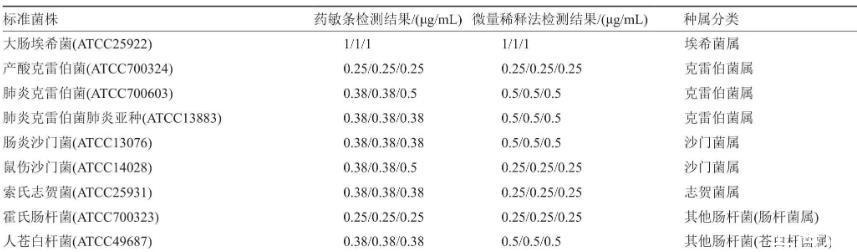
表1標準菌株重復3次檢測結果
相關新聞推薦
2、菌核凈與解淀粉芽孢桿菌Cas02生長曲線繪制,篩選出煙草赤星病防治效果更好的復配劑
